日本先進医療臨床研究会代表 小林 平大央
ガンをはじめとするさまざまな病気に効果大!大麻由来の薬とサプリメントとは?

ガンをはじめとするさまざまな難病に効果があり、鎮痛効果も高く、重度のてんかん症候群に著効とされる大麻由来の医薬品やサプリメントがあることをご存じでしょうか。大麻は日本や多くの国々で規制薬物に指定されていますが、欧米などでは医療用として大麻由来の医薬品やサプリメントの使用が許されています。こうした諸外国の動きに対応して、日本でも大麻由来の医薬品やサプリメントを取り巻く状況が変わりつつあります。
日本には、禁止薬物や規制薬物を取り締まる各種の法律があります。法規制を中心とした関係機関の連携による取り締まりのおかげで、日本での違法薬物使用の生涯経験率は諸外国と比較して非常に低く、欧米各国の20~40%と比べて日本では1.8%にとどまるなど、大きな成果を挙げています。
大麻は世界で最も乱用されている薬物であり、世界で150以上の国と地域が批准している国際条約「麻薬に関する単一条約」において、条約の制定当初から最も厳格な規制対象として位置づけられています。しかし、WHO(世界保健機関)の勧告によって、国連麻薬委員会において大麻から製造された医薬品の医療用途などへの活用を一定程度認める措置としてカテゴリーの変更が行われました。こうした変更を受けて、諸外国において大麻から製造された医薬品が申請を許可されはじめたのです。
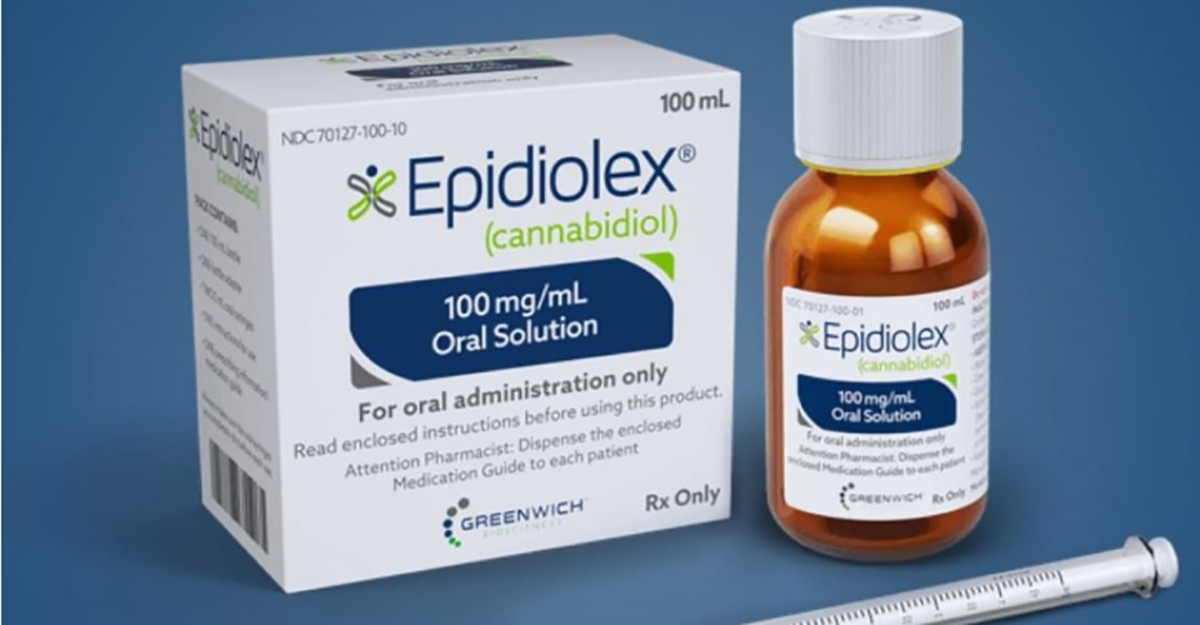
英国のGWファーマシューティカルズ社が開発した医薬品で大麻草を原料に抽出・精製された大麻成分のCBD(カンナビジオール)を主成分とする経口液剤「Epidiolex(エピディオレックス)」が米国FDAによって2018年6月に重度のてんかん症候群であるレノックス・ガストー症候群とドラベ症候群の治療薬として承認され、同年11月から米国で発売が開始されました。また、2019年9月には欧州委員会もエピディオレックスを承認し、欧州でも販売が開始されました。さらに、2020年にはエピディオレックスが米国FDAによって結節性硬化症の治療薬としても追加承認されています。
エピディオレックスは米国をはじめとするG7諸国において承認されていますが、日本においては大麻取締法に基づく大麻製品であることから輸入が原則禁止されています。大麻取締法では、所持や栽培は禁止されていますが、使用は禁止されていません。そのため、日本においても大麻から製造された医薬品の治験は、大麻研究者である医師の下、適切な実施計画に基づいて行えば可能です。ただし、現行の法規制では、大麻由来の医薬品の効果が認められて医薬品医療機器等法に基づく承認がなされたとしても、大麻の所持が許されないために医療現場で活用することは困難です。
こうした社会や国際情勢を踏まえて、日本でもやっと大麻を取り巻く状況に変化が起こりはじめました。2023年に大麻取締法の改正案が国会に提出され、改正の審議が行われる予定になったのです。
報告書で示された改正のポイントは、大きく次の三点です。
①麻向法(麻薬及び向精神薬取締法)に規定される免許制度などの流通管理のしくみの導入を前提として、大麻由来医薬品の製造や施用・受施用を可能とすること
②大麻の使用に対する罰則を設けること
③大麻草の部位による規制から成分に着目した規制に見直すこと
要するに、①大麻由来の医薬品であっても許可されたものは医療現場で使用できるようにする、②大麻使用の罰則を付加することで有害作用を持つ大麻使用の心理的な垣根を高くする、③現行の部位規制は問題が多いので有害成分であるTHC(テトラヒドロカンナビノール)を含まないように規制の見直しをする、といった内容です。
③についてさらに具体的にいうと、例えば欧米では大麻の有害作用を及ぼすTHCの含有率が一定の割合を超えた場合には「マリファナ」として規制し、それ未満は工業用の大麻として「ヘンプ」という名称で区別しています。この割合は国によって違い、例えば米国やオーストリア、チェコなどでは0.3%、英仏独では0.2%としています。
こうした諸外国の状況を背景に、日本でもTHCの成分規制は0.2%程度で決まるのではないかと推測されています。来年度以降、大麻取締法の改正案が可決されれば、有害成分THCが一定割合未満の医薬品やサプリメントが日本でも販売開始されることは間違いないでしょう。
ところで、大麻由来の合法製品を販売するために最も重要なことは、正確な検査をしてTHCの含有量が基準未満であることを証明することです。ところが、実はここに大きな問題があります。
現在、大麻の花や葉、根が禁止部位であり、これらの部位に多く含有されるTHCはいわば違法薬物です。現行の大麻取締法では、THCの所持が許されていないため、日本国内の検査施設はどこもTHCを測れないのです。そのため、来年の法改正を視野に入れてTHC含有率0.2%未満の製品を製造するには、米国などの検査施設を活用するしかないのです。
日本先進医療臨床研究会では、大麻由来の治療素材であるCBDにガンの疼痛緩和をはじめ、さまざまな効果・効能があることは分かっていたものの、大麻由来の医薬品やサプリメントに関しては問題があったことからCBDを使用した治療研究を行ってきませんでした。しかし、来年度以降は法律が改正されて合法的に医療現場での使用が解禁となることを想定し、基準をクリアした製品で治療効果が高いとされる高濃度のCBDを含有する製品を使用した治療研究を始めるべく準備を進めています。
もう一つの問題である検査体制についても、法令違反などで会員医師や患者さんに迷惑がかからないよう、米国で評価が高く実績のある検査施設と提携することで正確な検査を行い、基準をクリアした当会の認証製品だけを使用した治療研究を開始する予定です。
日本先進医療臨床研究会ホームページ



